| HUMIDADE DO AR |
18/07/2012 |
HUMIDADE DO AR
Embora a água esteja presente na atmosfera, em maior ou menor quantidade, a sua presença é geralmente invisível, porque se encontra sob a forma de vapor. De vez em quando, no entanto, condensa-se, formando nuvens que fornecem alguns indícios acerca da evolução do estado do tempo.
A água entra na atmosfera pelos processos de evaporação e de transpirarão. Mais tarde, volta à terra sob a forma de precipitação e, assim, completa o ciclo da água (ciclo hidrológico).
Para compreendermos estes processos e prevermos o futuro estado da atmosfera, temos de estudar as variações que ocorrem na humidade e estudar os métodos utilizados a para medir.
O ar húmido. Além dos componentes do ar seco, indicados no quadro 2-1 a atmosfera contém uma quantidade variável de vapor de água.
A mistura de ar seco e vapor de água chama-se ar húmido. Antes de estudarmos as características do ar húmido ternos de considerar alguns dos processos pelos quais a água passa de um estado para outro.
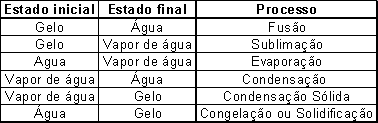
Os três estados da água. Como já foi referido anteriormente, a água à semelhança de muitas outras substâncias existentes na Terra, pode aparecer nos três estados da matéria. Para a água os três estados são os seguintes: - estado sólido – gelo; estado líquido – água; estado gasoso - vapor de água.
A água pode passar de um estado para outro, quer directa quer indirectamente. Os processos pelos quais a água passa de um estado para outro são: fusão; sublimação; evaporação; condensação; condensação sólida e congelação ou solidificação.
A tensão de vapor do ar húmido. A atmosfera é uma mistura de gases, exercendo cada um deles a sua pressão própria, que é chamada pressão parcial. A pressão parcial exercido por cada gás é proporcional ao número de moléculas do gás presentes no volume da mistura gasosa considerado.
À medida que a água se evapora para o ar seco, o vapor começa a exercer a sua própria pressão parcial, a que se chama tensão do vapor de água (e). A pressão atmosférica (p) aumenta, porque é agora igual à soma das pressões exercidos, tanto pelo vapor de água, como pelo ar seco.
Variações no conteúdo de vapor de água na atmosfera. A quantidade de vapor de água presente na atmosfera varia no tempo e no espaço. Regra geral, o teor de vapor de água aumenta sempre que a temperatura do ar aumenta e diminui quando a temperatura do ar sofre uma diminuição. Os valores mais elevados da tensão do vapor de água (cerca de 30 hPa) verificam-se nos trópicos junto à superfície do mar.
Os valores mais baixos à superfície do globo verificam-se nas regiões elevadas do interior do continente antárctico, durante os meses de Inverno, quando o ar está muito frio.
Em média, a tensão do vapor de água decresce quando a altitude aumenta. No entanto, pode por vezes ocorrer um aumento com a altitude, em certas regiões da atmosfera.
A tensão de saturação do ar húmido. Consideremos uma superfície plana de água, a um dada temperatura. Algumas das moléculas do líquido que têm movimento mais rápido escapam-se, geralmente da superfície da água para atmosfera, pelo processo de evaporação.
Algumas delas regressam à água, enquanto outras se deslocam, sob a forma de gás, no espaço sobrejacente à água.
Acabará por se atingir um momento em que o número de moléculas que regressa à água em cada segundo é igual ao número das que se escapam. Diz-se então que o espaço imediatamente acima da água está saturado para a temperatura a que se encontra esse espaço.
A tensão de vapor exercida pelo vapor de água num volume de ar saturado chama-se tensão de saturação à temperatura desse volume de ar.
A tensão de saturação varia com a temperatura. Quando o ar aquece, é necessária uma quantidade maior de moléculas de vapor de água para saturar o espaço sobrejacente ao líquido. Consequentemente, a pressão parcial exercida pelo vapor de água é superior. O ar tropical, quente, tem maior capacidade de retenção do vapor de água do que o ar polar frio. É, portanto, na vizinhança dos rios, lagos e oceanos tropicais que se verificam tensões de saturação elevadas.
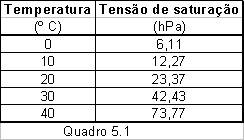
O quadro indica algumas tensões de saturação típicas sobre superfícies de águas planas, com diversas temperaturas.
O processo de condensação. Se se permitir a entrada de mais vapor num espaço já saturado a uma dada temperatura, ocorrerá condensação do vapor de água.
Há outros factores que afectam a condensação na atmosfera. A condensação ocorre sobre pequenas partículas em suspensão na atmosfera. Estas são conhecidas por núcleos de condensação e incluem poeiras, fumo, sal marinho, iões etc.
A condensação em certos núcleos ocorre com tensões de vapor inferiores à tensão de saturação para uma superfície plana de água pura à mesma temperatura. Alguns núcleos de condensação, tais como os núcleos salinos, têm também uma forte tendência para absorver a água, o que favorece a condensação. Chamam-se núcleos higroscópicos.
Na atmosfera há geralmente condensação em resultado do arrefecimento do ar húmido, isto é, ar que contém vapor de água. Quando a temperatura baixa, é necessária uma menor quantidade de vapor de água pára o ar ficar saturado. Eventualmente, atinge-se uma temperatura para a qual a tensão de vapor real se torna igual à tensão de saturação. Qualquer arrefecimento subsequente provoca a condensação.
Processos isobáricos. As relações entre a pressão, a temperatura e o volume dos gases foram estabelecidos a partir das primeiras experiências da física. Em algumas experiências conservou-se constante a pressão do gás. Um processo físico em que a pressão de um gás permanece constante chama-se um processo isobárico. A palavra "isobárico" significa de igual pressão.
É também possível estudar os processos isobáricos que ocorrem no ar húmido. Nestes processos aquece-se ou arrefece-se uma amostra de ar húmido mantendo-se constante a pressão. Não se permite a entrada ou saída de vapor de água da amostra de ar. Além disso, supõe-se que o vapor de água permanece no estado gasoso.
Quando o ar é arrefecido isobaricamente (isto é, a pressão constante), atinge-se uma temperatura para a qual ele fica saturado. Esta temperatura é conhecida por temperatura do ponto de orvalho ou, simplesmente, ponto de orvalho.
A temperatura do ponto de orvalho pode ser definida como a temperatura a que tem de ser arrefecida uma amostra de ar húmido, a pressão constante, para se atingir a saturação. Se a temperatura do ar baixar para além do ponto de orvalho, ocorrerá a condensação.
Processos de congelação. A água pura, no estado líquido, desde que não seja agitada, pode arrefecer até temperaturas inferiores ao ponto de congelação (0º C), continuando no estado líquido. Diz-se então que está em sobrefusão.
A introdução de um cristal de gelo, ou de qualquer núcleo de cristalização, fará com que se verifique a congelação da água sobrefundida. A congelação ocorrerá também se as gotículas de água em sobrefusão forem agitadas.
Experiências laboratoriais mostram que a temperatura mais baixa a que podem existir gotículas em sobrefusão é de cerca de -40º C. Abaixo desta temperatura a água congela, mesmo na ausência de núcleos de congelação.
Processos de condensação sólida (ou deposição). O processo pelo qual o vapor de água passa directamente a gelo, sem passar pelo estado líquido, chama-se condensação sólida. Por vezes este efeito é descrito como sublimação, mas este termo também se usa para descrever a passagem inversa, isto é, do estado sólido para o gasoso.
A condensação sólida não é tão vulgar como a condensação. Os núcleos em que tem lugar a condensação sólida são menos numerosos do que os núcleos de condensação e chamam-se núcleos de sublimação.
Sabe-se que a tensão de saturação em relação ao gelo é ligeiramente menor do que em relação à água em sobrefusão à mesma temperatura, como está indicado no quadro 5.2 para superfícies planas.
A temperatura do ponto de congelação é a temperatura a que uma amostra de ar húmido tem de ser arrefecida a pressão constante, para ficar saturada em relação a uma superfície plana de gelo. Se o ar húmido for arrefecido para além do ponto de geada, o vapor de água pode depositar-se, sob a forma de gelo, sobre certos objectos sólidos, incluindo outras superfícies de gelo ( isto é, sobre núcleos de sublimação).
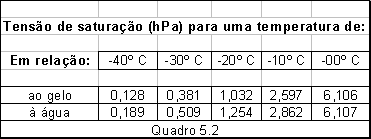
Do quadro 5-2, poderia parecer possível que a condensação sólida se produzisse enquanto o ar não está saturado em relação à água a essa temperatura. Na atmosfera, no entanto, as partículas de gelo das nuvens geralmente não aparecem enquanto não se atinge a saturação em relação à água. Supõe-se que a condensação se dá primeiro sobre um certo tipo de núcleos de condensação. Se estes forem de um tipo que também actue como núcleos de congelação, a água sobre eles condensada pode então congelar. Há ainda algumas dúvidas quanto ao modo como estes núcleos provocam a congelação, mas parece que uma das propriedades essenciais dos núcleos reside em a estrutura da película de água que resulta da condensação se assemelha à de um cristal de gelo.
Por outro lado, pode já haver por vezes cristais de gelo presentes, que tenham talvez caído de nuvens geladas existentes a níveis superioras. Se a tensão de saturação for superior à tensão de saturação em relação ao gelo, verificar-se-á então a condensação sólida directa sobre os cristais de gelo.
Calor latente. Para fazer uma substância mudar de estado é necessário adicionar ou subtrair calor a essa mesma substância. Enquanto se realiza a mudança de estado, o calor adicionado não altera a temperatura.
Por exemplo, à pressão normal de uma atmosfera, a água começa a ferver a 100º C. Enquanto esta passa do estado liquido ao gasoso, a temperatura não sobe embora se adicione calor, Este calor é necessária para separar as moléculas e é conhecido por calor latente de vaporização.
O calor latente ou "escondido" é de novo libertado quando o vapor de água volta, por condensação, ao estado líquido. De maneira semelhante, é necessário o calor latente de fusão para fundir o gelo e este calor liberta-se, mais tarde, quando a água congela, transformando-se de novo em gelo.
Indicadores de humidade. Usa-se a palavra humidade para descrever qualquer medida da quantidade de vapor de água contida numa dada porção da atmosfera. Por exemplo, esta quantidade é por vezes expressa directamente como a massa de vapor de água na unidade de volume do ar. Por outro lado, pode ser descrita indirectamente pela contribuição que o vapor de água dá à pressão total de todos os gases atmosféricos.
Um importante indicador de humidade é a humidade relativa.
Humidade relativa. A humidade relativa é um indicador de humidade conveniente. É a proporção entre a massa de vapor de água realmente presente na unidade de volume de ar e a necessária para saturar esse ar à mesma temperatura. A humidade relativa é geralmente expressa em termos de percentagem.
Se o ar não está saturado, a massa de água presente por unidade de volume é sensivelmente proporcional á tensão de vapor. Portanto, a humidade relativa pode ser determinada a partir da relação:
Note-se que a humidade relativa pode alterar-se, mesmo que o conteúdo de vapor de água se mantenha constante. Este fenómeno ocorre se se alterar a temperatura da amostra de ar. Nestas circunstâncias, a humidade relativa tende a atingir o valor mais elevado pela madrugada, quando a temperatura do ar atinge o mínimo. Em algumas situações, pode atingir-se a saturação no ar. Se ocorrer a condensação pode formar-se neblina ou nevoeiro. Quando a temperatura sobe, já durante o dia, a humidade relativa decresce e a neblina ou nevoeiro desaparece.
Métodos de medição da humidade. Os instrumentos utilizados na medição da humidade ou conteúdo de vapor de água chamam-se higrómetros. Vamos considerar os diferentes meios pelos quais se pode  determinar a humidade do ar num dado local. determinar a humidade do ar num dado local.
As dimensões de certas substâncias orgânicas alteram-se quando varia a humidade relativa do ar. Este efeito é utilizado em alguns higrómetros. Por exemplo, o cabelo humano varia de comprimento quando a humidade relativa varia. Estas alteraras podem ser amplificados por um sistema de alavancas e utilizadas para fazer deslocar um ponteiro. É o princípio do higrómetro de cabelo.
Pode obter-se um registo continuo da humidade relativa do ar se o ponteiro for substituído por uma pena que trace a indicação num gráfico ligado a um tambor cilíndrico, em rotação. Este instrumento chama-se higrógrafo de cabelo.
Um método simples, mas rigoroso, de medir a humidade consiste na utilização de um psicrómetro. Este instrumento é constituído simplesmente por dois termómetros montados um ao lado do outro, um dos quais mede a temperatura do ar e o outro a temperatura do termómetro molhado.
Por vezes chama-se ao psicrómetro um higrómetro de termómetro seco e termómetro molhado. O termómetro molhado é idêntico ao termómetro seco vulgar, utilizado na medição da temperatura atmosférica. No entanto, o reservatório é coberto por uma camada fina de musselina de algodão, conservada molhada por meio de uma torcida de fios de algodão grosso, mergulhada num pequeno recipiente com água destilada. Os termómetros seco e molhado devem ser ventilados e protegidos da radiação solar.

Uma vez obtidas as temperaturas do termómetro seco e do termómetro molhado, podem usar-se tabelas para determinar a humidade relativa ou temperatura do ponto de orvalho.
Densidade do ar húmido. A densidade do ar seco varia com a pressão e a temperatura. Junto à superfície terrestre, à pressão normal de uma atmosfera (1013,25 hPa) e à temperatura de l5º C (288,15º K), a densidade do ar é de 1,225 Kg/m3.
Como está indicado no quadro 2.1, o ar seco é uma mistura de gases. Não existe, portanto, molécula de ar seco propriamente dita. No entanto, é possível determinar o peso molecular médio do ar seco que é, por vezes, chamado "peso molecular aparente do ar seco". Na atmosfera, em que os gases estão todos misturados, este valor é de cerca de 28,96.
O vapor de água, por outro lado, tem um peso molecular sensivelmente igual a 18. Este valor é só cerca de 5/8 do peso molecular médio do ar seco na região da atmosfera que se estende até à Mesopausa, onde a mistura dos gases é homogénea e a sua composição é aproximadamente constante. A molécula da água tem, portanto, uma massa inferior à da "molécula média" do ar seco.
Suponhamos agora que substituímos algumas das moléculas de um dado volume de ar seco por um número equivalente de moléculas de vapor de água. A massa do volume de gás ficará, então, reduzida, donde se conclui que a densidade do ar húmido é inferior à do ar seco à mesma pressão e temperatura.
Textos: CAP\TOMET Fernando Garrido sob manual MDINT 395/12 FAP
Fotos e desenhos: CAP\TOMET Fernando Garrido
|